
(2)反响III中偏铝酸钠和二氧化碳反响生成氢氧化铝沉积和碳酸氢钠;氢氧化铝受热分化生成氧化铝和水蒸气且吸收热量,氧化铝熔点较高,一般条件下不熔融;
(3)二氧化硅和HF反响生成H2SiF4和水.答复:解:硅藻土中含有二氧化硅和有机质及少数的Al2O3、Fe2O3、MgO等杂质,这些物质中只要有机物能不免;
(1)粗硅藻土高温不免过程中只要有机质不免,其它物质不发生反响,所以粗硅藻土高温不免的意图是除掉有机质,故答案为:除掉有机质;
(2)反响III中偏铝酸钠和二氧化碳反响生成氢氧化铝沉积和碳酸氢钠,反响方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3;氢氧化铝受热分化生成氧化铝和水蒸气且吸收热量,氧化铝熔点较高,一般条件下不熔融,所以氢氧化铝可以作阻燃剂,
故答案为:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3;氢氧化铝分化吸收热量,且生成高熔点的氧化铝掩盖在外表;
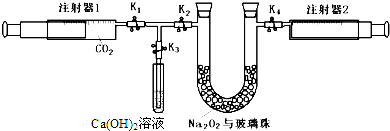
注射器1中抽取了100mLCO2,U型管中装有适量小玻璃珠和约1.5gNa2O2粉末.试验开始时,翻开KI、K2、K4止水夹,封闭K3止水夹推进注射器1活塞,慢慢将CO2压至U型管,注射器2活塞慢慢向外移动.答复下列问题:(本题不考虑注射器内壁的磨擦阻力)
(1)U型管内的玻璃珠并不参加反响,其所起的效果除避免过氧化钠粉末被吹走外,另一个及其重要的效果是.
(3)注射器1活塞推究竟后,注射器2中收集到的气体大于50mL,其原因除或许仍还含CO2外,还有一个重要原因是.
②近似以为0.50mol?L-1NaOH溶液和0.55mol?L-1盐酸溶液的密度都是1g?cm-3,中和后生成溶液的比热容c=4.18J?g-1?℃-1,且测得温度的均匀升高值是3.4℃,请核算中和热△H=kJ?mol-1(取小数点后一位).
③上述试验数值成果与57.3kJ?mol-1有误差,成果误差或许的原因或许是(填字母).
④假如用60mL0.5mol?L-1氢氧化钠溶液与50mL0.55mol?L-1盐酸溶液进行反响,与上述试验比较,所放出的热量(填“持平”或“不持平”),所求的中和热(填“持平”或“不持平”)(假定两种情况下试验操作完全相同)
(1)X在周期表中的方位:,其原子核外有种不一样的形状的电子云.这五种元素中,最外层有两个未成对电子的元素是(用元素符号标明).
(2)常温下液态化合物甲只含上述元素中的两种,分子中原子个数比1:1,甲的电子式是.
(5)X的氧化物是构成光化学烟雾原因之一,工业上可采用它与其氢化物反响生成无毒害物质而除掉,请用方程式标明该反响.
(5)写出C在高温度高压力、催化剂条件下与足量氢氧化钠水溶液充沛反响的化学方程式:
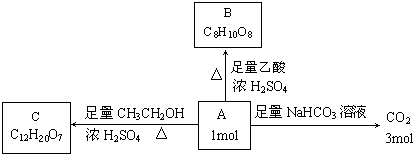
(2)核磁共振氢谱标明A分子中有4个氢处于完全相同的化学环境.则A的结构简式是.
上一篇:硅藻泥主要成分是什么
下一篇:用途极广的绿色环保材料